차세대 항암제로 주목받고 있는 CAR-T 제조에 있어 미국에서는 약효보다 안전성에 더 중점을 두는 것으로 알려졌다. 특히 이는 최근 의약품 부실 관리로 인해 많은 사고를 유발하고 있는 국내 상황에도 시사하는 바가 크다.
바이오코리아 2018 기간 중인 10일 열린 컨퍼런스에서는 항암치료제로 큰 주목을 받고 있는 CAR-T의 인허가 대응전략에 대한 강의가 있었다.
이 세션은 메디포스트 사업개발본부 이승진 본부장의 좌장아래 Car-T의 미국 내 시장 동향 및 유럽시장 내 유전자 치료제의 최신 허가 동향에 대한 발표 등이 진행됐다.
Axteria Biomed Consulting Inc의 Principle Consultant인 Gunang Gao는 CAR-T제조 및 테스트에 있어 美 FDA의 가이드에 대한 주제로 강의를 펼쳤다.

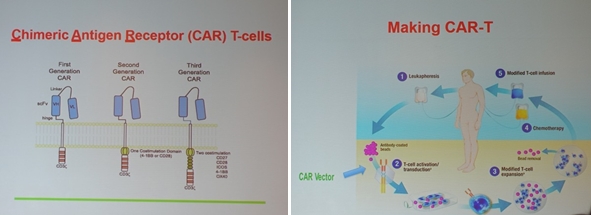
우선 CAR-T 치료는 환자에게 T세포를 추출해서 이 T세포에 환자의 암세포 표면에 있는 항원과 결합하는 수용체 정보를 입력한 후 다시 환자 몸속에 투여해 환자의 암세포를 찾아가 공격하여 암을 치료하는 방식의 세포치료제이다.
강의 내용에 따르면 미국 FDA는 CAR-T에 대한 가이드라인을 2015년 제정됐다. 따라서 이를 확인하고 CAR-T 제조 및 테스트를 시작해야 한다.
가이드에 따르면 각 단계별 테스트가 있으며 이를 통해야 비로소 최종 프로덕트가 나올 수 있다.
이 과정 중 첫째는 FDA가 가장 중요하게 보는 ‘안전성’이다. “이는 무균성을 확인하는 것으로, 가이드라인을 반드시 준수해야 안전성을 자신 있게 제시할 수 있다”며 “FDA는 제품을 안전하게 만들기 위해 가장 큰 노력을 하므로 안전성을 약효보다 더 중요하게 본다”는 것.
둘째는 ‘Identity’로 가이드에 제시된 행정적 절차에 따라 잘 관리하고 환자에게 주입해야 한다는 것이 골자다.
셋째는 ‘Purity’ 즉, 순도 부분이다. 구체적으로는 T셀이 80% 이상의 순도를 가지고 있어야 하고, 불순물 세포가 포함됐을 때는 어떤 불순물이 들어있고 어떻게 제거할 수 있는지 정의해야 한다.
넷째는 ‘Potency’ 효능 부분이다. 환자에게서 추출한 세포를 다시 치료제로 주입할 때 효능을 주장하기 위해서는 어떤 부분을 근거로 두고 주장하는지 증빙문서가 필요하다.
마지막으로는 ‘Final Product Specification-example’과 ‘Lot Release Specification -example’가 제시돼야 한다.
Gunang Gao는 “FDA에서는 치료제를 임상 현장에 전달하기까지 표준운영절차(SOPs)가 적용되고 있는지. 운송할 때도 적절한 SOPs에 맞춰 운송하고 관리하고 있는지를 확인하므로 이 모든 과정에 대해 문서화해야 한다”고 조언했다.
한편, CAR-T셀 제조가 다른 생물학적 제제보다 어려운 점에 대해서도 설명했다.
CAR-T셀 제조과정의 모든 장비는 FDA의 승인을 받은 장비를 사용해야 하며, 그렇지 않은 경우는 직접 검증을 거쳐야 한다. 또 CAR-T가 체외에서 조작한 세포이므로 마지막 과정서 살균을 할 수 없으므로 전체 과정에서 무균으로 진행 돼야 한다는 점이다. 이같이 전체 무균 과정을 확인해야 하며, 제조과정 중 리스크에 대해 분석해야 한다. 즉, 어떤 위험이 있는지 파악하고 저감 방법을 기술해야 하며, 이를 운영하는 직원들도 교육해야 한다.
또 한 가지 고려할 사항은 CAR-T셀을 제조할 때는 모든 루트 하나하나를 테스트해야 한다는 제한 사항이 있다는 것이다. 그러나 어떤 테스트는 오래 걸리기도 하며, 그러면 제품 출시에 지장이 있을 수 있다. 이 같이 제품 출시를 위해선 정해진 기간 내에 빨리 마쳐야하는데 이를 어떻게 극복할 수 있을까? 이에 대해서는 “테스트에 대해 유연성, 융통성 가져야 한다”는 것. “우선은 테스트 결과를 빨리 받도록 해야 하며, 일부 테스트가 오래 걸리면 조건부 출시를 할 수도 있다”면서 “결과적으로 제품을 제때 공급하려면 SOPs를 잘 정의해서 제출해야 한다”고 재차 강조했다.
즉 정리하면, 제조에서 물류까지 SOPs가 잘 적용되고 있는지 검토해야 하며, 생산능력도 고려해야 한다. 또한 현장에 교육 받은 오퍼레이터가 얼마나 되는지, 운송 단계에서 액체 질소로 포장되어 잘 운송되고 있는 지 모든 것을 기록에 남겨야 한다. 그 다음 단계로 어떻게 포장과 라벨 하는지, 최종 포장 검사에서 라벨이 섞이지 않게 바코드 시스템도 잘 점검해야 한다고 조언했다.

